| |
Кортикальный зрительный протез
диссертация Марианны Ивановой
статья "Свет в конце нейрона" журнал Эксперт, 2008г
Табл. 1. Характеристика экспериментальной группы животных
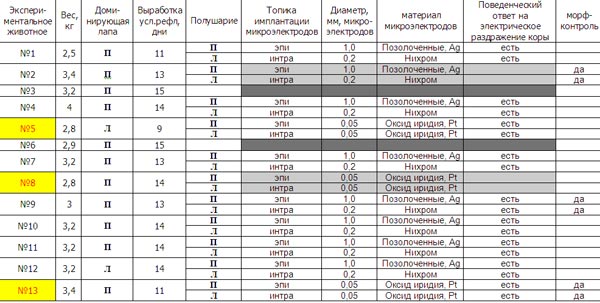
На основе переноса периферического условного рефлекса в центральный нами была разработана нейрофизиологическая модель для исследования крайних значений параметров электрического раздражения зрительной коры головного мозга, при которых возникают фосфены.
На рис. 1.А отображено животное с установившимся условным рефлексом поднятия лапы в ответ на предъявление МФП в фиксирующем жилете в экспериментальной камере. Затем животному надевали повязку (рис. 1, Б), которой зашторивали глаза, и которая не мешала дышать. 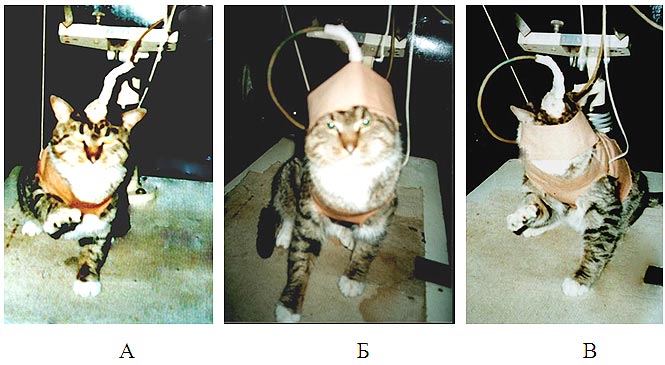
Рис. 1. Представление разработанной нейрофизиологической поведенческой модели.
Затем проводили электрическую стимуляцию коры головного мозга различными параметрами, и в некотором их диапазоне животное поднимало лапу (рис. 1, В) точно так же, как и при предъявлении «модели фосфенного поля».
Все параметры, которые были изменяемы в ходе эксперимента по электрической стимуляции, представлены на рис. 2. Обозначены параметры самой составляющей МКИ кортикального зрительного протеза (топика имплантации, диаметр микроэлектродов и количество стимулируемых микроэлектродов от 1 до 8), указаны параметры, изменение величин которых проводили дискретно, опираясь на данные литературы (частота раздражения, полярность импульса и длительность трейна импульсов). Интервалами указаны наиболее значимые параметры для возникновения фосфенов (сила тока, сопротивление одиночного электрода, общее сопротивление стимулируемых микроэлектродов и длительность импульса).
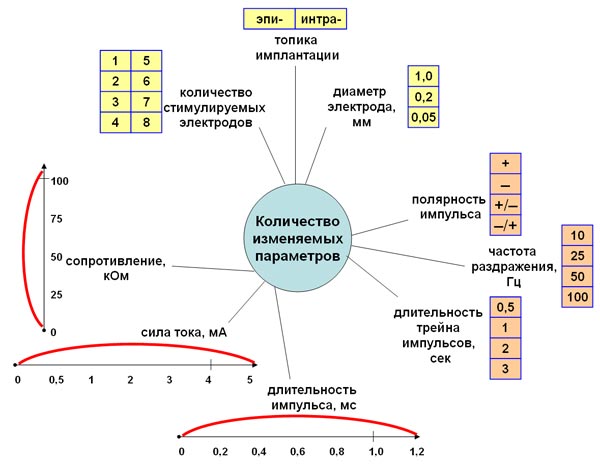
Рис. 2. Схема, отображающая три группы изменяемых параметров при стимуляции электродов. В ходе эксперимента был получен поведенческий ответ животного при параметрах, диапазон которых указан на рис. 3.
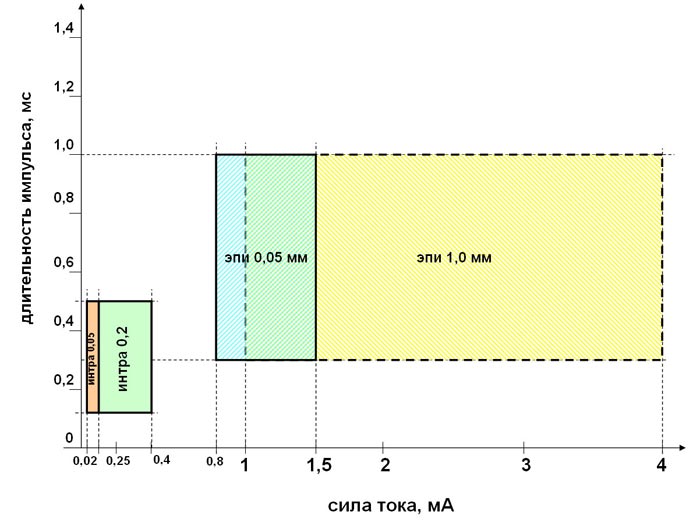
Рис. 3. Связь диапазонов длительностей импульса (мс) и силы тока (мА), при которой наблюдается четкий поведенческий ответ на возникновение фосфенов при различной топике имплантации (эпи-, интракортикальной) и диаметра микроэлектрода (0,05, 0,2 или 1,0 мм .) при фиксированной частоте раздражения 100 Гц, длительности двухполярного -/+ трейна импульсов 1,0 с и четырех произвольно выбранных микроэлектродах. Изучение сопротивления микроэлектродов. В группе эпикортикальной имплантации 1,0 мм электродов в среднем сопротивление через 7 дней после имплантации составило 2,1±1,7 кОм, через 1 месяц после имплантации – 9,2±5,3 кОм, через 8 месяцев после имплантации 21,3±9,0 кОм. В группе эпикортикальной имплантации микроэлектродов 0,05 мм сопротивление через 7 дней после имплантации составило 12,3±4,9 кОм, через 1 месяц после имплантации – 19,8±8,1 кОм, через 8 месяцев после имплантации 50,2±32,1 кОм.
В группе интракортикальной имплантации 0,2 мм электродов сопротивление через 7 дней после имплантации составило 3,2±1,7 кОм, через 1 месяц после имплантации – 8,4±3,1 кОм, через 8 месяцев после имплантации 16,5±7,2 кОм. В группе интракортикальной имплантации 0,05 мм микроэлектродов сопротивление через 7 дней после имплантации составило 9,3±5 кОм, через 1 месяц после имплантации – 14,1±7 кОм, через 8 месяцев после имплантации 47,7±30 кОм.
Имеет место тенденция значительного увеличения сопротивления электродов и микроэлектродных матриц со временем. Измеренные данные в 1 и 8 месяц достоверно отличаются. В связи с повышением сопротивления со временем приходится подавать все большее напряжение для достижения порога индукции фосфена. В табл. 2 приведены сводные данные напряжения, по результатам наших измерений во всех исследуемых животных при различной локализации имплантации электродов и их диаметре.
Срок имплантации
Группа животных
|
7 дней |
1 месяц |
8 месяцев |
Эпи- 1,0 мм (I = 2,5 мА) |
5,0 |
22,5 |
52,5 |
Эпи- 0,05 мм (I = 1,2 мА) |
14,8 |
23,8 |
60,2 |
Интра- 0,2 мм (I = 0,3 мА) |
0,96 |
2,52 |
4,95 |
Интра- 0,05 мм (I = 0,0 6 мА) |
0,56 |
0,85 |
2,8 |
Табл. 2. Усредненные параметры напряжения (В), которые необходимо подавать на электроды и микроэлектроды для индукции фосфенов в зависимости от длительности нахождения их в ткани мозга.
Таким образом, напряжение, которое необходимо подавать на электроды, за 8 месяцев повышается в несколько раз, что затрудняет использование имплантированных электродов в качестве зрительного протеза в течение длительного времени. Необходимо решить вопрос возрастания общего сопротивления, прежде чем переходить к серийным исследованиям на добровольцах. Итак, в заключение приведем обобщенные параметры электрического раздражения, при которых был получен поведенческий ответ от животного (табл. 3).
Параметры раздражения
Электроды, диаметр, мм |
Сила тока, мА |
Длительность импульса, мс. |
Полярность импульсов |
Частота, Гц |
Длит-ть трейна, с. |
Напряжение, В (средн.) |
Импеданс, кОм |
Интракортикальные, 0,2 |
0,1 – 0,4 |
0,1 – 0,5 |
Однополярный
Двухполярный |
25-100 |
1 – 2 |
0,96 |
3 – 8 |
Эпикортикальные, 1,0 |
1 – 4 |
0,3 – 1,0 |
Однополярный
Двухполярный |
25-100 |
1 – 2 |
5,0 |
2 – 9 |
Интракортикальные, 0,05 |
0,02 – 0,1 |
0,1 – 0,5 |
Однополярный
Двухполярный |
25-100 |
1 – 2 |
0,56 |
9 – 14 |
Эпикортикальные, 0,05 |
0,8 – 1,5 |
0,3 – 1,0 |
Однополярный
Двухполярный |
25-100 |
1 – 2 |
14,8 |
12 – 20 |
Табл. 3. Параметры раздражения электродов в экспериментальной группе животных, вызывающие перцепцию фосфенов и поведенческий ответ.
Далее >> Обсуждение результатов
Актуальность ::: Обзор литературы (ч.1) (ч.2) ::: Методы ::: Результаты ::: Обсуждение и выводы ::: Литература
(с) Марианна Иванова
|
|